La química inorgánica es la rama de la química que estudia la formación, composición, estructura y reacciones de los compuestos inorgánicos, es decir, aquellos que no contienen enlaces carbono-hidrógeno. A simple vista, puede parecer que es un campo muy técnico y alejado de la vida diaria, pero lo cierto es que está presente en múltiples aspectos de nuestro entorno.
A lo largo de este artículo exploraremos 🔎 qué es la química inorgánica, en qué se diferencia de la orgánica, cómo se clasifican los compuestos inorgánicos, cuáles son sus propiedades y reglas básicas de nomenclatura.
3000 a.C. – 500 d.C.
🏺 Antigüedad
Uso de metales como oro, cobre y hierro Desarrollo de la metalurgia y fabricación de vidrios y pigmentos
Siglos VIII–XV
⚗️ Edad Media
Desarrollo de la alquimia Descubrimiento y uso de ácidos minerales
1661
📘 Robert Boyle
Nacimiento de la química moderna con enfoque experimental
1789
🔥 Antoine Lavoisier
Ley de conservación de la masa Definición moderna de elemento químico
1803
⚛️ John Dalton
Formulación de la teoría atómica
1869
📊 Dmitri Mendeléyev
Creación de la tabla periódica Predicción de nuevos elementos
Principios del siglo XX
🔬 Teoría del enlace químico
Desarrollo de modelos para explicar enlaces iónicos y covalentes Avances en estructura atómica y química de coordinación
Segunda mitad del siglo XX
🏭 Era de los nuevos materiales
Desarrollo de catalizadores industriales, semiconductores y cerámicos avanzados Expansión de la química organometálica
Siglo XXI
🔋 Nanotecnología y sostenibilidad
Investigación en nanomateriales y energías renovables Desarrollo de baterías avanzadas y aplicaciones biomédicas

¿Qué es la química inorgánica?
Tradicionalmente se ha definido por oposición a la químia orgánica, pero, hoy en día, se entiende como un campo con identidad propia 🗣️. Se centra en el análisis de las propiedades y transformaciones de los compuestos inorgánicos, aunque su definición exacta es:
La química inorgánica se encarga del estudio integrado de la formación, composición, estructura y reacciones químicas de los elementos y compuestos inorgánicos.

¿Cuál es su objeto de estudio?
- La composición química de las sustancias
- La estructura atómica y molecular de los compuestos
- Las propiedades físicas: punto de fusión, densidad o conductividad
- Las propiedades químicas: reactividad y estabilidad
- Las reacciones químicas que experimentan
Aademás, la química inorgánica analiza cómo infuyen factores como la temperatura 🌡️, la presión o el medio en el comportamiento de estos compuestos.
Como cualquier otra ciencia, la química inorgánica mantiene una relación estrecha con otras áreas. Esto significa que, además de química inorgánica como tal, tendrás que estudiar y comprender otras ramas:
Química orgánica
Estudian distintos tipos de compuestos, pero ambas comparten principios fundamentales sobre enlaces y reacciones
Química analítica
Permite identificar y cuantificar sustancias inorgánicas mediante técnicas experimentales
Fisicoquímica
Aporta las bases teóricas para comprender la energía, la termodinámica y la cinética de las reacciones inorgánicas
Diferencias entre química inorgánica y química orgánica
La principal diferencia entre ambas ramas está en el tipo de compuestos que estudian 📖. Mientras que la química orgánica se centra en compuestos que contienen enlaces carbono-hidrógeno (C-H), la química inorgánica, como ya sabes, estudia aquellas que no presentan este tipo de enlace (al menos, como estructura principal).
| 🧪 Tipo de compuesto | 📘 Definición básica | 📑 Ejemplos | ✔️ Aplicaciones principales |
|---|---|---|---|
| Óxidos metálicos | Compuestos formados por un metal y oxígeno | Óxido de calcio (CaO), óxido de hierro (Fe₂O₃) | Construcción (cemento), producción de acero, pigmentos |
| Óxidos no metálicos | Compuestos formados por un no metal y oxígeno | Dióxido de carbono (CO₂), dióxido de azufre (SO₂) | Industria alimentaria (bebidas carbonatadas), producción de ácidos |
| Ácidos hidrácidos | Ácidos sin oxígeno, formados por H + no metal | Ácido clorhídrico (HCl), Ácido sulfhídrico (H₂S) | Industria química, tratamiento de metales, procesos industriales |
| Oxoácidos | Ácidos que contienen hidrógeno, oxígeno y otro elemento | Ácido sulfúrico (H₂SO₄), Ácido nítrico (HNO₃) | Fertilizantes, baterías, fabricación de explosivos |
| Bases fuertes | Sustancias que liberan OH⁻ completamente en agua | Hidróxido de sodio (NaOH), Hidróxido de potasio (KOH) | Fabricación de jabones, detergentes, papel |
| Bases débiles | Liberan OH⁻ parcialmente en solución | Hidróxido de aluminio (Al(OH)₃) | Antiácidos, tratamiento de aguas |
| Sales binarias | Formadas por un metal y un no metal | Cloruro de sodio (NaCl), Sulfuro de hierro (FeS) | Alimentación, procesos metalúrgicos |
| Sales ternarias | Contienen metal, no metal y oxígeno | Sulfato de cobre (CuSO₄), Nitrato de potasio (KNO₃) | Agricultura (fertilizantes), fungicidas, pólvora |
| Compuestos de coordinación | Compuestos con un metal central unido a ligandos | [Cu(NH₃)₄]²⁺, [Fe(CN)₆]³⁻ | Catálisis, análisis químico, medicina |
| Compuestos metálicos | Elementos metálicos con enlace metálico | Hierro (Fe), Cobre (Cu) | Construcción, electricidad, maquinaria |
Así, en la química inorgánica predominan los enlaces iónicos (como en muchas sales), los enlaces covalentes (como en algunos óxidos) y los enlaces metálicos (como en los metales puros). En la química orgánica, en cambio, predominan los enlaces covalentes entre átomos de carbono y otros elementos como hidrógeno, oxígeno o nitrógeno.
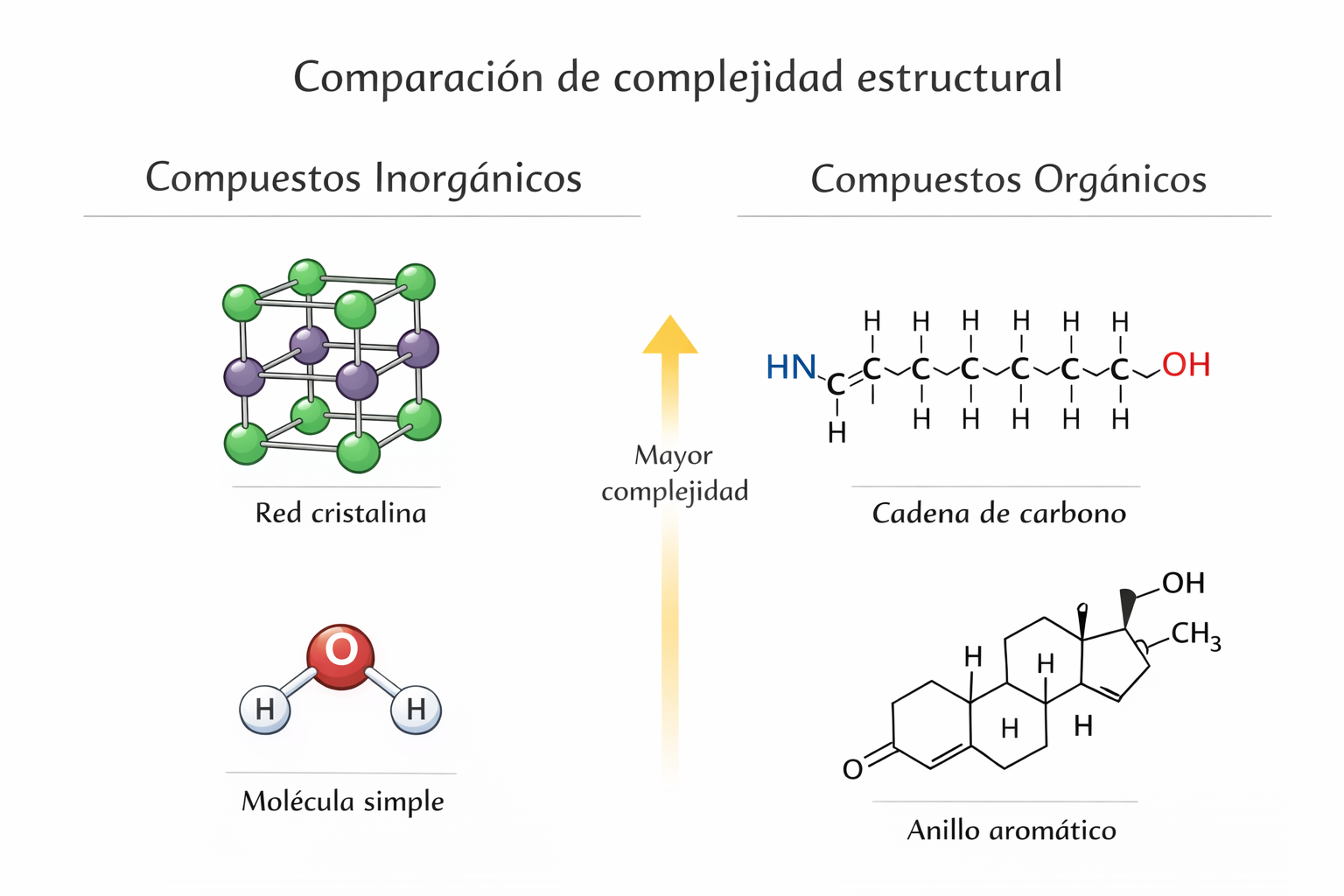
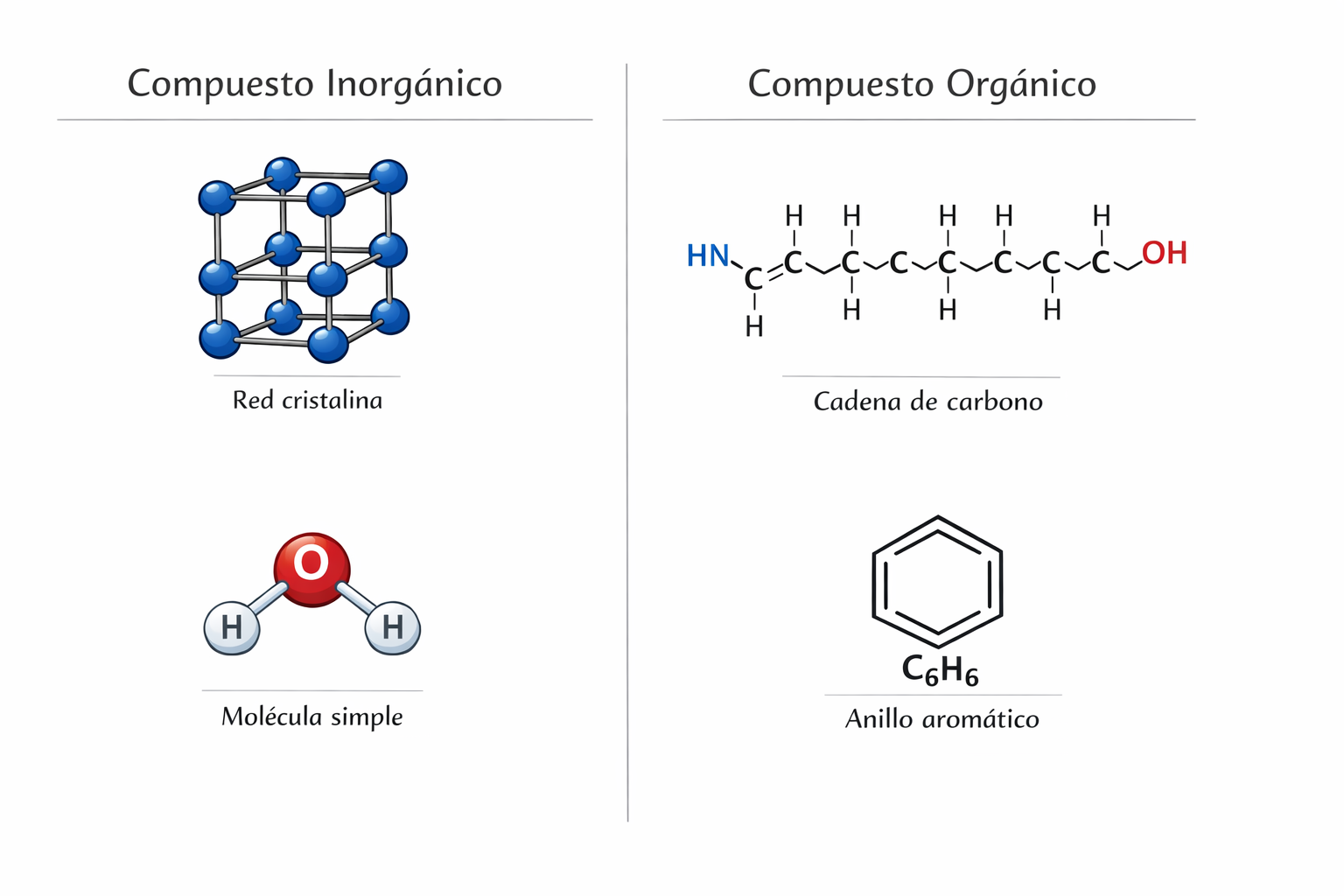
Las moléculas orgánicas suelen tener estructuras complejas; en la inorgánica, es frecuente encontrar estructuras más simples ✔️. Ojo: eso no le resta sofisticación. Si no te aclaras, ¡siempre es mejor preguntar a tu profesor o profesora de las clases particulares de quimica!

Clasificación general de los compuestos inorgánicos
Los compuestos inorgánicos se clasifican según su composición química y su comportamiento frente a otras sustancias. Entre los principales grupos se encuentran: óxidos, ácidos, bases y sales.
Óxidos
Compuestos formados por la combinación de un elemento con oxígeno.
Hay dos tipos de óxidos: los metálicos (formados por un metal y oxígeno) y los no metálicos (formados por un no metal y oxígeno).
Ejemplos 👇
- Óxido de calcio (CaO), un óxido metálico que se utiliza en la construcción.
- Dióxido de carbono (CO₂), un óxido no metálico presente en la respiración y la combustión.
Ácidos
Sustanciass que liberan protones (H⁺) en solución acuosa, según la teoría de Brønsted-Lowry.
Hay dos tipos de ácidos: los hidrácidos (formados por hidrógeno y un no metal y sin oxígeno) y los oxoácidos (contienen hidrógeno, oxígeno y otro elemento central).
Ejemplos 👇
- Ácido clorhídrico (HCI), utilizado en la industria y presente en el jugo gástrico.
- Ácido sulfúrico (H₂SO₄), ampliamente utilizado en procesos industriales.
Con estos química inorgánica ejemplos se ve mucho más clara la importancia de esta ciencia.
Bases
Sustancias que liberan iones hidiróxido (OH⁻) en solución acuosa o que aceptan protones.
Hay dos tipos de bases: las fuertes (se disocian completamente en agua) y las débiles (se disocian parcialmente).
Ejemplos 👇
- Hidróxido de sodio (NaOH), utilizado en la fabricación de jabones.
- Hidróxido de calcio (Ca(OH)₂), empleado en construcción y tratamiento de aguas.
Sales
Compuestos formados por la reacción entre un ácido y una base, en un proceso llamado neutralización.
Hay dos tipos de sales: las binarias (formadas por un metal y un no metal) y las ternarias (contienen un metal, un no metal y oxígeno).
Ejemplos 👇
- Cloruro de sodio (NaCI), la sal común de mesa.
- Sulfato de cobre (CuSO₄), utilizado en agricultura y laboratorio.
¿Sabías que puedes recurrir a nuestros ejercicios de química inorgánica para repasar antes de un examen? ¡Échales un vistazo!
Propiedades generales de los compuestos inorgánicos
Los compuestos inorgánicos presentan una gran variedad de propiedades físicas, que son las siguientes:
- Estado de agregación: muchos son sólidos a temperatura ambiente, aunque también existen líqudios 💧 y gases 💨.
- Solubilidad: algunas sales son solubles en agua 🌊, mientras que otras no.
- Dureza: muchos compuestos iónicos forman sólidos duros y frágiles ⚱️.
- Conductividad: los metales conducen electricidad ⚡ en estado sólido, mientras que las sales lo hacen cuando se funden o se disuelven.
Asimismo, hay que entender las propiedades químicas más relevantes, entre las que destacan:
- Reactividad: algunos metales reaccionan fácilmente con el oxígeno 🌬️ o el agua.
- Comportamiento ácido-base: los compuestos pueden actuar como ácidos ⚗️, bases o sustancias neutras.
- Estabilidad: ciertos compuestos son muy estables 💪, mientras que o tros se descomponen con facilidad.
Estudiar estas propiedades permite prever cómo reaccionará una sustancia ante determinadas condiciones.
Nomenclatura básica de los compuestos inorgánicos
Si has estudiado química antes, sabrás que la nomenclatura química es el sistema que permite nombrar los compuestos de forma sistemática y universal. Dicho sistema se basa en reglas establecidas por la Unión Internacional de Química Pura y Aplicada (IUPAC). Algunos principios incluyen:
Prefijos
para indicar la cantidad de átomos
Sufijos
según el tipo de compuesto
N.º de oxidación
cuando un elemento presenta varias valencias

Nomenclatura de óxidos
- «Óxido de» seguido del nombre del elemento
- Si el elemento tiene varias valencias, se indica con números romanos entre paréntesis.
FeO: óxido de hierro (II)
Fe₂O₃: óxido de hierro (III)
Nomenclatura de ácidos, bases y sales
- Ácidos hidrácidos: «ácido» + raíz del no metall + «hídrico»
- Oxoácidos: sufijos como «-oso» o «-ico» según la valencia.
- Bases: «hidróxido de» + nombre del metal.
- Sales: derivan del nombre del ácido correspondiente, cambiando los sufijos según el caso
La química inorgánica, lejos de ser una disciplina abstracta, es en realidad uno de los pilares fundamentales de la ciencia moderna 🔬. No importa si hablamos de los materiales que dan forma a nuestras ciudades o de los procesos industriales que sostienen la economía global: el estudio de estaciencia es imprescindible para entender y transformar el mundo en el que vivimos.
Nuestro profesor de quimica online te compartirá su pasión por este mundo.
📚 Bibliografía
- Brown, T. L., LeMay, H. E., Bursten, B. E., Murphy, C., Woodward, P., & Stoltzfus, M. (2014). Química: La ciencia central (12.ª ed.). Pearson Educación.
- Greenwood, N. N., & Earnshaw, A. (1997). Chemistry of the elements (2nd ed.). Butterworth-Heinemann.
- Miessler, G. L., Fischer, P. J., & Tarr, D. A. (2014). Inorganic chemistry (5th ed.). Pearson.
- Atkins, P., & Jones, L. (2012). Principios de química: Los caminos del descubrimiento (5.ª ed.). Editorial Médica Panamericana.
- IUPAC. (2019). Compendium of chemical terminology (the “Gold Book”). International Union of Pure and Applied Chemistry. https://goldbook.iupac.org
Resumir con IA:


























